细胞周期与凋亡检测试剂盒
产品描述:
细胞周期是指细胞从一次分裂完成开始到下一次分裂结束所经历的全过程,主要分为细胞分裂间期与有丝分裂期(M 期)两个阶段;细胞间期主要由 DNA 合成前期(G1 期)、DNA合成期(S期)与 DNA 合成后期(G2 期)组成,整个细胞周期变化顺序可用 G1→S→G2→M来表示。首先 G1 时期:细胞主要合成 RNA 和蛋白质等物质,为细胞进入 S 期做好物质和能量的准备;随后进入 S 期:细胞开始进行 DNA 和一些组蛋白等物质合成,细胞 DNA 含量开始增加;最后到G2期:这时细胞 DNA 含量已经变成了 G1 时期的 2 倍,并已经停止了 DNA 的复制,为进入有丝分裂期做大量的蛋白质等物质的合成;如果 G0(细胞暂时停止分裂和分化期、静止期)/G1 期,细胞中DNA含量为 1N;那么处于 G2 期的细胞中 DNA 含量为 2N; 而处于 G1 和 G2 时期之间的S期细胞,DNA 含量在 1N~2N 之间;而凋亡的细胞,细胞核会发生浓缩和 DNA 片段化,导致部分基因组 DNA 片段丢失,所以其 DNA 含量是小于 1N 的,在流式检测的荧光图上出现所谓的sub-G1峰,即凋亡细胞峰。因此,可根据细胞 DNA 的含量来判断细胞所处的周期和状态。细胞凋亡也可以用流式细胞仪观察细胞光散射的变化来检测。细胞发生凋亡时,由于胞浆和染色质浓缩、核碎裂,产生凋亡小体,使细胞的光散射性质发生变化。凋亡前期,染色质皱缩,细胞密度增加,前向角光散射色显著降低;凋亡后期,细胞产生凋亡小体,前向角光散射和侧向角光散色均显著降低。细胞周期与凋亡检测试剂盒(Cell Cycle and Apoptosis Analysis Kit)采用了经典的碘化丙啶染色(Propidium staining)方法对细胞周期与凋亡进行检测分析。利用碘化丙啶能够嵌入双链 DNA 中,并使其产生荧光,并且荧光强度和双链 DNA 的含量成正比的特性;结合细胞不同周期中,DNA 含量的规则变化, 可以区分细胞处于的周期和状态。本试剂盒可用于组织细胞、贴壁或悬浮细胞的细胞周期与凋亡检测(如用于组织的细胞周期与凋亡检测,则须把组织消化成单细胞状态,才可进行检测)。
储存与运输
冰袋(wet ice)运输;-20℃避光保存,染色缓冲液可 4℃保存;
有效期
12 个月有效。
组成: (50次)

操作步骤:
1. 细胞样品准备(细胞数量控制在 1×105~1 ×106 个)
1.1. 贴壁细胞:去除培养液,加入胰蛋白酶消化液消化细胞,在显微镜下观察到细胞变圆松动,加入适量含血清的细胞培养基终止消化,轻轻吹散细胞,将细胞制成悬液;将悬液转移至离心管中,1000 g 离心 3-5 min,弃上清,保留细胞沉淀;再用预冷 PBS 缓冲液润洗1-2 次细胞沉淀,同样方法离心弃上清,保留细胞沉淀。
1.2. 悬浮细胞:直接将细胞转移至离心管中,1000 g 离心 3-5 min,弃上清,保留细胞沉淀;再用预冷 PBS 缓冲液润洗 1-2 次细胞沉淀,同样方法离心弃上清,保留细胞沉淀。
1.3. 组织细胞:将组织尽量剪切成小块,根据组织来源,选择胰酶、胶原酶等消化酶消化组织块,并用 100-300 目筛网过滤,得到单细胞悬液;将过滤后的细胞悬液转到离心管中,1000g离心 3-5 min,弃上清,保留细胞沉淀;再用预冷 PBS 缓冲液润洗1-2 次细胞沉淀,同样方离心弃上清,保留细胞沉淀。
2. 细胞样品固定
2.1. 向收集的细胞沉淀样品中加入 1 mL 冰上预冷的 75 %乙醇,轻轻吹打细胞,使其充分接触;
2.2. 将细胞置于 4℃固定 30 min 或更长时间(通常固定 2 h 或以上更能保证染色效果,固定 12-24 h 可能效果更佳,可提高染色效果)。
2.3. 固定一定时间后,将细胞 1000 g 离心 3-5 min,去除乙醇固定液,保留细胞沉淀;
2.4. 轻敲离心管底部,使细胞分散,用 PBS 缓冲液重悬并洗涤细胞,1000 g 离心3-5 min,弃上清收集细胞沉淀;
3. 染色工作液的配制与染色
3.1. 根据下表避光配制染色工作液,配制量可以根据使用需求,等比例增加或减少(配制完成的染色工作液短时间内可以 4℃保存,请当日内使用);
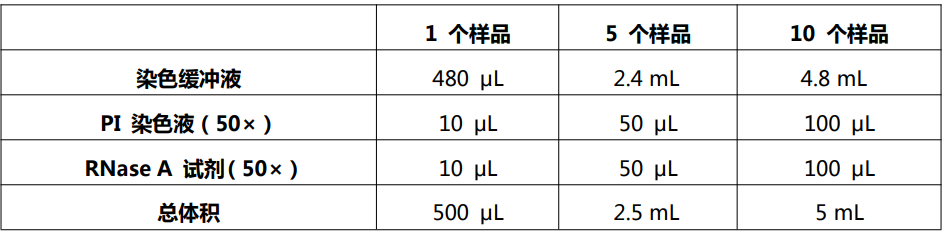
3.2. 轻敲离心管底部,使步骤 2.4 中沉淀的细胞分散,再加入 500 μL 配制好的染色工作液,轻轻吹打,使细胞分散并与染色工作液混匀;
3.3. 37℃避光孵育 30 min,即可用流式细胞仪进行检测。
4. 流式检测和分析
用流式细胞仪在激发波长 488nm 波长处检测红色荧光,同时检测光散射情况。采用适当分析软件进行细胞 DNA 含量分析和光散射分析。
注意事项 :
1.荧光染料均存在荧光淬灭问题,使用和保存过程中尽量避光;
2.在实验前建议对细胞进行周期同步化处理,避免细胞所处周期不同导致的较大重复性差异;
3.实验细胞种植密度不宜过高也不宜过低,以防出现接触抑制或密度依赖等现象;
4.操作 PI 染色液时应注意防护,避免直接接触人体或吸入体内;
5.操作时请穿实验服,佩戴一次性手套。
 在线客服1号
在线客服1号